地址:新乡经济技术开发区经十一路与纬七路交叉口中开企业城独栋厂房A12号101室
联系人:刘经理
手机号:13462234439
手机号:15617189811
技术联系人:刘国敏
手机号:18560210809
邮箱:yifeigl@163.com
河南一飞过滤机械有限公司
液氨的合成工艺设计
1 前言
1.1 液氨的性质、用途及其价格
液氨为无色气体,有刺激性恶臭味。分子式NH3。分子量17.03。相对密度0.7714g/l。熔点-77.7℃。沸点-33.35℃。自燃点651.11℃。蒸气密度0.6。蒸气压1013.08kPa(25.7℃)。蒸气与空气混合物爆炸极限16~25%(**易引燃浓度17%)。氨在20℃水中溶解度34%,25℃时,在无水乙醇中溶解度10%,在甲醇中溶解度16%,溶于氯仿、乙醚,它是许多元素和化合物的良好溶剂。水溶液呈碱性,0.1N水溶液PH值为11.1。液态氨将侵蚀某些塑料制品,橡胶和涂层。遇热、明火,难以点燃而危险性较低; 但氨和空气混合物达到上述浓度范围遇明火会燃烧和爆炸,如有油类或其它可燃性物质存在,则危险性更高。与硫酸或其它强无机酸反应放热,混合物可达到沸腾
液氨主要用于生产硝酸、尿素和其他化学肥料,还可用作医药和农药的原料。在国防工业中,用于制造火箭、导弹的推进剂。可用作有机化工产品的氨化原料,还可用作冷冻剂。
NH3分子中的孤电子对倾向于和别的分子或离子形成配位键,生成各种形式的氨合物。如[Ag(NH3)2]+、[Cu(NH3)4]2+、BF3·NH3等都是以NH3为配位的配合物。
液氨是一个很好的溶剂,由于分子的极性和存在氢键,液氨在许多物理性质方面同水非常相似。一些活泼的金属可以从水中置换氢和生成氢氧化物,在液氨中就不那么容易置换氢。但液氨能够溶解金属生成一种蓝色溶液。这种金属液氨溶液能够导电,并缓慢分解放出氢气,有强还原性。例如钠的液氨溶液: 金属液氨溶液显蓝色,能导电并有强还原性的原因是因为在溶液中生成“氨合电子”的缘故。例如金属钠溶解在液氨中时失去它的价电子生成正电子:
液氨加热至800~850℃,在镍基催化剂作用下,将氨进行分解,可以得到含75%H2、25%N2的氢氮混合气体。用此法制得的气体是一种良好的保护气体,可以广泛地应用于半导体工业、冶金工业,以及需要保护气氛的其他工业和科学研究中。
今年10月下旬以来,由于前期价格过高及下游需求减弱,液氨价格是呈现明显的下跌趋势,出厂报价大多在2800-3600元(吨价,下同),下跌幅度在150-300元。黑龙江、吉林、浙江等地价格相对较高,河北、河南、安徽等地价格相对较底。
11月30日,国家发改委宣布自12月1日起上调销售电价和上网店家,销售电价全国平均每千瓦时上调3分钟。许多省份化肥电价上调幅度高于平均水平,上调幅度大多在4分钱左右,高的如湖北等地超过了六分钱。液氨是好点大户,每生产一吨液氨,约耗电1500千瓦时,相当于增加液氨成本60元左右,高的达到近百元。由于目前液氨价格已近低点,成本上涨将推动液氨价格走高。另外,尿素、、碳酸氢铵等下游产品价格反弹,对液氨价格有所支撑。但由于目前液氨市场仍然偏弱,价格反弹至前妻高点的可能性不大。
经过了12月上中旬的短暂上涨后,12月下旬,液氨价格重现跌势,元旦过后,市场也未见好转,继续下跌。目前液氨出厂价格大多为2700-3500元(吨价,下同),河北价格相对较低,现金提货出厂价格大多为2700-2850元,安徽、江苏出厂报价大多在3000元左右,个别低的出厂价在2850元左右,黑龙江前期价格一直较高,个别高的厂家出厂报价3800元,目前也回落到了3400元左右。
1.2 液氨的生产历史及发展前景
液氨的系统理论研究始于上世纪三十年代,正式投入工业化生产是在上世纪七十年代,**初于1963年挪威逊克斯塔尔里莎大学和挪威中央工业研究所共同开发的液氨加工工艺,当时还是从纱线整理入手,以替代纱线丝光处理的技术。由于液氨对纱线有着极强的渗透性,残留在纱线上的氨液比碱液更易于去除,而且比碱液丝光效果更好,因而引起重视。1968年美国桑福公司获得后,冠以桑福纯棉牛仔布(Sanfor-set)**面世,成衣尺寸稳定,手感柔软的牛仔布风行一时。但是到了上世纪七、八十年代,一方面合纤迅速发展,市场上各类涤棉产品易洗快干深受消费者青睐,另一方面又伴有返朴回真、回归大自然的潮流,纯棉织物颇受大众喜爱。液氨整理主要是美国用以整理厚重牛仔布织物,加以液氨整理技术复杂,氨回收要求高,而且成本又十分昂贵,因此国内外市场几度周折普及甚缓,后来导致美国至少有七台液氨整理设备相继搁置起来,还有一台迁移至泰国。在上世纪八十年代的这段时间里液氨整理加工,在国内外市场上确定沉寂了十来年,直至上世纪九十年代,日本主要一些企业为了启动市场、开发产品,在液氨整理工艺设备的基础上,着力进行了树脂整理工艺技术的创新改进,结合液氨整理积极研发了形态稳定整理技术,虽历经多次失败,终于在1993年日清纺推出了超级柔软整理(S.S.P.),与此同时东洋纺也推出了气相整理(V.P.),此时日本市场打出了纯棉免烫整理产品,几乎半数的衬衣都要经过形态稳定整理加工,这些工艺都是在液氨整理的基础上再进行树脂整理,一时市场上掀起了形态稳定整理的热潮。日本京都机械和山东铁工厂已经可以提供液氨整理机,前川制作所和岩谷产业已经可以提供配套的液氨回收装置。此时美国对液氨整理似乎遗忘了,而此时日本却对液氨整理加工技术又重新复苏。
我国是1982年上海第二印染厂从美国莫里森公司引进一套液氨整理技术设备和回收装置,可以说在二十世纪里,我国仅仅引进过这一套液氨整理设备。当时包括支付费和设备费等投入资金相当可观,后来在品种开发、氨的回收、市场销售等方面未能取得满意的效果,因而始终未能形成规模生产,就是在这样的多种因素的背景下,国内各方面对推广应用液氨整理技术持慎重观望态度,但也有地区对这项新技术一直抱有热忱,1985年河南省把液氨整理技术列入省内技术攻关项目,由新乡印染厂和河南省纺科院以及有关院校合作,历经四年多时间收集资料、认真研究、消化吸
收,终于1992年由企业自行设计研制了我国**台液氨整理样机,就是在这台机器上新乡印染厂十多年来一直坚持生产,摸索了许多宝贵的经验,相继开发出许多品种,如纯棉牛仔布、大麻舒爽呢、麻/棉混纺织物等,享有一定声誉,应该说河南省相关企业和单位对我国开发液氨整理工艺技术和设备奠定了有益的基础,对我国印染行业后整理做出了贡献。
还有值得欣喜的是在1996年江阴一家规模不算大的民营澄江纺织机械厂,原来主导产品是空压机,对液氨整理设备从未接触过,经过三年多时间进行调研,足迹遍及十多个省市,协同河南省纺科院专家组织访问、足坛、消化、吸收,在技术严格封锁保密的情况下,千方百计掌握技术资料,在产、学、研结合下,在新乡印染厂和河南纺科院十多年先行一步的基础上,以及协同南京化工大学的专家、老师共同探索液氨整理设备和回收装置的性能特点,借助化工技术的强项,攻克一系列技术难关,终于在世纪之交的1999年成功地制造了一台具有我国特色的高科技液氨整理机和回收装置。澄江纺织机械厂只是一家民营企业,在资金十分困难的条件下,以厂房抵押作了“破釜沉舟”的决心,为了保证项目的成功开发,坚定不移地走“科技联姻、技术合作”的路子。该机胜利制成后安装在江阴康源印染厂投入生产,在2000年元月由中国纺机器材工业协会组织的现场交流会上,全国近二十家印染企业的专家进行了实地考察和评价,一致认为该设备在较短时间内克服种种困难创制成功,是我国纺机企业自行设计制造的一件大事,即使由于种种原因,未能继续投入第二台设备,但是辛勤和艰苦卓绝的劳动成效,不能不让人们仍然记忆着此功不可没。 到了世纪之交年代,国内印染行业注意到近年来日本一些大公司,在积极发展纯棉形态稳定整理和技术中添置了液氨整理设备,此时正是国内在“九五”规划结尾和“十五”规划酝酿阶段,看中了其对纯棉产品具有改善穿着舒适和免烫效果的时尚,液氨整理一时成了一些企业的热点,有意向要引进液氨整理项目的不下十多家,涉及全国八、九个省市,有的请国外相关公司来介绍,有的组织去国外考察,有的还进行了可行性报告的研究。经过一段时间的广泛听取多方面意见和进一步市场调研,逐渐有了比较正确地认识,一些企业也重新作了规划,**后具体落实并付诸实施的有宁波雅戈尔日中纺织印染有限公司和山东鲁泰纺织股份有限公司,都已经投入了批量生产,并为我国开发纯棉免烫产品开辟了市场,树立了**。许多企业的认识也不断深化,比较能结合本企业的实际和市场需求,全面客观地应对企业的技术改造。
化学模拟生物固氮的重要研究课题之一,是固氮酶活性中心结构的研究。固氮酶由铁蛋白和钼铁蛋白这两种含过渡金属的蛋白质组合而成。铁蛋白主要起着电子传递输送的作用,而含二个钼原子和二三十个铁和硫原子的钼铁蛋白是络合N2或其他反应物(底物)分子,并进行反应的活性中心所在之处。关于活性中心的结构有多种看法,目前尚无定论。从各种底物结合物活化和还原加氢试验来看,含双钼核的活性中
心较为合理。中国有两个研究组于1973—1974年间,不约而同地提出了含钼铁的三
核、四核活性中心模型,能较好地解释固氮酶的一系列性能,但其结构细节还有待根据新的实验结果精确化。
**上有关的研究成果认为,温和条件下的固氮作用一般包含以下三个环节:
①合过程。它是用某些过渡金属的有机络合物去络合N2,使它的化学键削弱;
②还原过程。它是用化学还原剂或其他还原方法输送电子给被络合的N2,来拆开N2中的N—N键;
③氢过程。它是提供H+来和负价的N结合,生成NH3。
化学模拟生物固氮工作的一个主要困难是,N2络合了但基本上没有活化,或络合活化了,但活化得很不够。所以,稳定的双氮基络合物一般在温和条件下通过化学还原剂的作用只能析出N2,从不稳定的双氮络合物还原制出的NH3的量相当微少。因此迫切需要从理论上深入分析,以便找出突破的途径。
固氮酶的生物化学和化学模拟工作已取得一定的进展,这必将有力地推动络合催化的研究,特别是对寻找催化效率高的合成氨催化剂,将是一个有力的促进。
1.3 液氨的国内知名生产厂家及价格
南京君路化工有限公司,该公司位于中国南京沿江工业开发区,紧靠南京化工园,公司主要经营冰醋酸、氨水、苯胺、液碱、甲醇、甲醛、醋酸甲酯、醋酸乙酯、液氨等产品,畅销消费者市场,在消费者当中享有较高的地位,公司与多家大型化工厂家建立了长期稳定的合作关系。南京君路化工有限公司经销的冰醋酸、氨水、苯胺、液碱、甲醇、甲醛、醋酸甲酯、醋酸乙酯、液氨品种齐全。当前氨水价格≥15:700.00元/吨
山西长子丹峰化工有限公司,该公司始建于1976年,1996年扩规改造成4万吨合成氨/年,并进行了改制,产品主要有碳铵、液氨、甲醇和二甲醚。2008年形成6万吨总氨/年能力,2010年进行扩规改造,形成10.万吨总氨/年能力。
河北中冀化工集团河北中冀化工集团 成品材料加工商 :天 坡化工有限公司.总部设在:河北石家庄高新区.公司生产氨水/液氨/等化工产品.设备设施均采用**一流.公司成立运输公司拥有25辆运输车.月生产能力7000吨,当前价格:980元/吨。
南昌市宏伟气体有限公司,司位于环境优美、工业高速发展、经济繁荣的赣江之滨、京九线上的红色旅游胜地-南昌。本公司地处南昌市水产大市场,是一家销售液
体二氧化碳、液氧液氨液氮液氩工业丙烷干冰高纯乙炔气、高纯氧气、高纯二氧化碳、高纯氩气、高纯氦气、高纯氮气混合气、食品二氧化碳工业气高纯气、特种气体、稀有气体等。本公司创建于1996年,通过十几年来的不断完善我公司现已成为江西省具有一定规模的**销售性公司。现有员工50多人,各种运输车辆20余辆,为拓宽产品市场,面对新的挑战,公司坚持“诚信为本、务实求新”的经营理念,以管理创效益,以科技求发展,以服务拓市场,以质量树**
2工艺设计
2.1合成液氨的原则流程
合成氨的原料是氢气和氮气。氮气来源于空气,可以在制氢过程中直接加入空气,或在低温下将空气液化、分离而得;氢气来源于水或含有烃的各种燃料。工业上普遍采用的是以焦炭、煤、天然气、重油等燃料与水蒸气作用的气化方法。
原料→造气→净化→合成→分离→氨
↑ ▕
▔▔▔
循环气
图1 液氨合成的原则流程
(1)原料气制备 将煤和天然气等原料制成含氢和氮的粗原料气。对于固体原料煤和焦炭,通常采用气化的方法制取合成气;渣油可采用非催化部分氧化的方法获得合成气;对气态烃类和石脑油,工业中利用二段蒸汽转化法制取合成气。
(2)净化 对粗原料气进行净化处理,除去氢气和氮气以外的杂质,主要包括变换过程、脱硫脱碳过程以及气体精制过程。
① 一氧化碳变换过程
在合成氨生产中,各种方法制取的原料气都含有CO,其体积分数一般为12%~40%。合成氨需要的两种组分是H2和N2,因此需要除去合成气中的CO。变换反应如下:
CO+H2O→H2+CO2 ΔH =-41.2kJ/mol
由于CO变换过程是强放热过程,必须分段进行以利于回收反应热,并控制变换段出口残余CO含量。**步是高温变换,使大部分CO转变为CO2和H2;第二步是低温变换,将CO含量降至0.3%左右。因此,CO变换反应既是原料气制造的继续,又是净化的过程,为后续脱碳过程创造条件。
② 脱硫脱碳过程
各种原料制取的粗原料气,都含有一些硫和碳的氧化物,为了防止合成氨生产过
程催化剂的中毒,必须在氨合成工序前加以脱除,以天然气为原料的蒸汽转化法,**道工序是脱硫,用以保护转化催化剂以重油和煤为原料的部分氧化法,根据一氧化碳变换是否采用耐硫的催化剂而确定脱硫的位置。工业脱硫方法种类很多,通常是采用物理或化学吸收的方法,常用的有低温甲醇洗法(Rectisol)、聚乙二醇二甲醚法。
粗原料气经CO变换以后,变换气中除H2外,还有CO2、CO和CH4等组分,其中以CO2含量**多。CO2既是氨合成催化剂的毒物,又是制造尿素、碳酸氢铵等氮肥的重要原料。因此变换气中CO2的脱除必须兼顾这两方面的要求。
一般采用溶液吸收法脱除CO2。根据吸收剂性能的不同,可分为两大类。一类是物理吸收法,如低温甲醇洗法(Rectisol),聚乙二醇二甲醚法(Selexol),碳酸丙烯酯法。一类是化学吸收法,如热钾碱法,低热耗本菲尔法,活化MDEA法,MEA法等。
③ 气体精制过程
经CO变换和CO2脱除后的原料气中尚含有少量残余的CO和CO2。为了防止对氨合成催化剂的毒害,规定CO和CO2总含量不得大于10cm3/m3(体积分数)。因此,原料气在进入合成工序前,必须进行原料气的**终净化,即精制过程。
目前在工业生产中,**终净化方法分为深冷分离法和甲烷化法。深冷分离法主要是液氮洗法,是在深度冷冻(<-100℃)条件下用液氮吸收分离少量CO,而且也能脱除甲烷和大部分氩,这样可以获得只含有惰性气体100cm3/m3以下的氢氮混合气,深冷净化法通常与空分以及低温甲醇洗结合。甲烷化法是在催化剂存在下使少量CO、CO2与H2反应生成CH4和H2O的一种净化工艺,要求入口原料气中碳的氧化物含量(体积分数)一般应小于0.7%。甲烷化法可以将气体中碳的氧化物(CO+CO2)含量脱除到10cm3/m3以下,但是需要消耗有效成分H2,并且增加了惰性气体CH4的含量。甲烷化反应如下:
CO+3H2→CH4+H2O ΔH=-206.2kJ/mol
CO2+4H2→CH4+2H2O ΔH=-165.1kJ/mol
⑶氨合成 将纯净的氢、氮混合气压缩到高压,在催化剂的作用下合成氨。氨的合成是提供液氨产品的工序,是整个合成氨生产过程的核心部分。氨合成反应在较高压力和催化剂存在的条件下进行,由于反应后气体中氨含量不高,一般只有10%~20%,故采用未反应氢氮气循环的流程。
氨合成反应式如下:
N2+3H2→2NH3(g) ΔH=-92.4kJ/mol
2.2合成液氨的带控制点的工艺流程图及概述
由氮氢气压缩机送来的35℃~45℃的新鲜气,与放空后经冷交换器来的循环气混合,而后温度被降至20℃,进入氨冷器Ⅰ。气体管内流动,液氨在管外蒸发,由于氨大量蒸发吸收了混合气的热量,使管内气体进一步被冷却至0℃左右,为降低氨冷器Ⅰ负荷,进入氨冷器Ⅱ继续冷却至-15℃左右,出氨冷器后的气液混合物,在冷交换器的下部用分离器将液氨分离,分离出的液氨进入液氨贮罐,分氨后的循环气上升至上部换热器壳程被热气体加热至22℃后出冷交换器,然后,气体经循环压缩机,补充压力至15兆帕,由合成塔的下部进入层间换热器,移走第二绝热床反应热,冷气体升温进入**绝热床进行合成反应,再入**、二绝热床空间(冷激器)由185度左右的冷气体作冷激气原与出**绝热床的反应气体混合降温到385度左右,混合后气体进入第二绝热床进行合成反应,气体氨净值升高,出第二绝热床气体进入层间换热器,移走热量,使冷气升温,热气体降温后进入第三绝热床进行合成反应,气体氨含量增加到16.5﹪,再经塔内下换热器将热量移走,后进入沸热锅炉,副产1.3Mpa蒸气。换热产生蒸汽后进入循环器加热器一次出塔气体至160℃,本身温度降至112℃左右进水冷器被冷却产生部分液氨,温度降至35℃,混合气液进氨分离器,分离液氨,分离的液氨去液氨罐贮存,出氨分离器的气体则部分放空,放空气去氢回收装置,放空后的循环气经冷交换器降温至17℃与新鲜气混合,继续下一循环。液氨产品易蒸发,有强烈刺激性气味,对人的消化系统和呼吸系统都造成伤害,与空气混合后遇火会爆炸,应密闭贮存,管道输送,尽可能避免泄漏。
2.3合成液氨的工艺条件
影响氨合成反应速度因素:
1.压力 提高压力可加快氨的生成速度使气体中氨含量迅速增加。
2.温度 反应速度随着温度升高显著加快,如图2.1、2.2
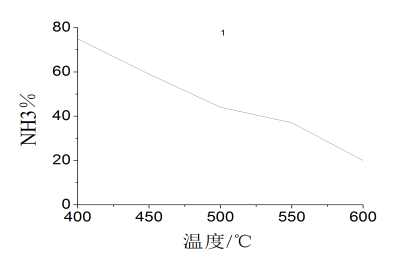
图3.1 平衡时氨产率与温度的关系
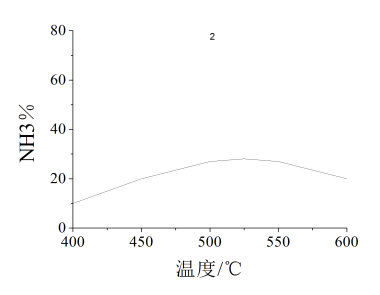
图3.2 经过一定时间反应后氨产率与温度的关系
3可行性分析
氨合成反应的特点:3H2+N2=2NH3+Q
(1)是可逆反应。即在氢气和氮气反应生成氨的同时,氨也分解成氢气和氮气。
(2)是放热反应。在生成氨的同时放出热量,反应热与温度、压力有关。
(3)是体积缩小的反应。
(4)反应需要有催化剂才能较快的进行。
3.1工艺可行性分析
3.1.1液氨合成的理论基础
从化学工艺的角度看其核心是反应过程工艺条件的确定,而确定反应的**佳工艺条件,需先从事反应热力学和动力的研究
⑴合成液氨反应的动力学
氨合成为气固相催化反应,它的宏观动力学过程包括以下几个步骤。
a.混合气体向催化剂表面扩散(外,内扩散过程);
b.氢,氮气在催化剂表面被吸附,吸附的氮和氢发生反应,生成的氨从催化剂表面解吸(表面反应过程);
c.氨从催化剂表面向气体主流体扩散(内,外扩散过程) 氮、氢气在催化剂表面反应过程的机理,可表示为:
N2(g)+Cate —→2N(Cate)
H2(g)+Cate —→2H(Cate)
N(Cate) + H(Cate) —→NH(Cate)
NH(Cate) + H(Cate) —→NH2(Cate)
NH2(Cate) + H(Cate) —→NH3(Cate)
NH3(Cate)—→NH3(g) + (Cate)
实验结果证明,N2活性吸附是**慢的一步,即为表面反应过程的控制步骤。
对整个气固相催化反应过程,是表面反应控制还是扩散控制,取决于实际操作条件。低温时可能是动力学控制,高温时可能是内扩散控制;大颗粒的催化剂内扩散路径长,小颗粒的路径短,所以在同样温度下大颗粒可能是内扩散控制,小颗粒可能是化学动力学控制
当内扩散控制时,动力学方程为rNH3=kP式中rNH3为反应速率,k为扩散系数,p为反应物的总压
⑵氨合成反应的热效应
氢气和氮气合成氨是放热,体积缩小的可逆反应,反应式如下:
0.5N2+1.5H2==NH3 ΔH0=46.22 kJ·mol-1
其反应热不仅与温度有关,还与压力和组成有关。表一为纯3H2-N2混合气生成φNH3为17.6%系统反应的热效应。
表一
P/MPa | 0.1 | 10.1 | 20.2 | 30.4 | 40.5 | |
t/℃
| 400 | 52.7 | 53.8 | 55.3 | 56.8 | 58.2 |
500 | 54.0 | 54.7 | 55.6 | 56.5 | 57.6 | |
⑶化学平衡常数
应用化学平衡移动原理可知,低温、高压操作有利于氨的生成。但是温度和压力对合成氨的平衡产生影响的程度,需通过反应的化学平衡研究确定。高压下化学平衡常数Kp值不仅与温度有关,而且与压力和气体组成有关。
研究者把不同温度、压力下K<s
- 上一篇:深能合和电力液氨储罐置换方案(外)
- 下一篇:没有了;





